02/18/2016
No.0284 タンパク質翻訳後の修飾位置の解析
タンパク質はリン酸基や糖鎖、脂質などにより翻訳後修飾され、細胞内のシグナル伝達や免疫系等において機能する。これらの修飾位置の解析は重要であるが確実な解析方法は確立されていない。ここでは糖タンパク質の糖結合位置及びリン酸化ペプチドのリン酸化部位のLCMS-IT-TOFを用いた解析例を紹介する。
●糖タンパク質(Fetuin)の糖鎖結合位置の解析
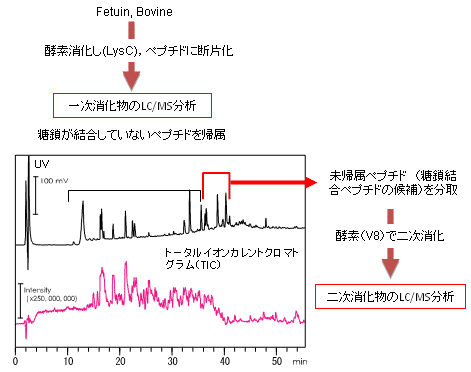
一次消化物のLC/MS分析
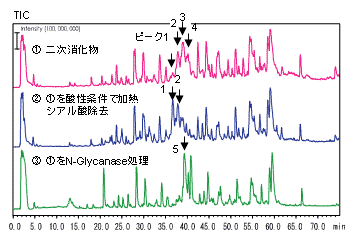
二次消化物のLC/MS分析
ピーク5:図4のペプチドの糖鎖が除去され、NがDに変わった質量を観測
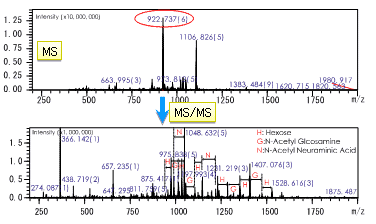
①のピーク3のMS/MS分析
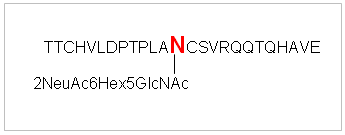
ピーク3の構造
上記ペプチドのアスパラギンに糖鎖が結合と決定
ピーク1,2,4:ピーク3のNeuAcの結合数が異なるもの
酵素消化、シアル酸除去処理及びN-Glycanase処理の3種類の試料について精密質量LCMS/MS分析を行い比較することにより、糖タンパク質の糖鎖結合位置の解析を確実に実施することができた。
●リン酸化ペプチドのリン酸化部位の解析
LCで分離した4本のピークのうちピークAの解析結果を以下に示した。
試料:4種類のリン酸化ペプチドの混合標準品
方法:ニュートラルロスサーベイ(NLS)
※NLS: MS/MS分析で特定のニュートラルロスの判定を行い,そのイオンのMS3分析を行うモード
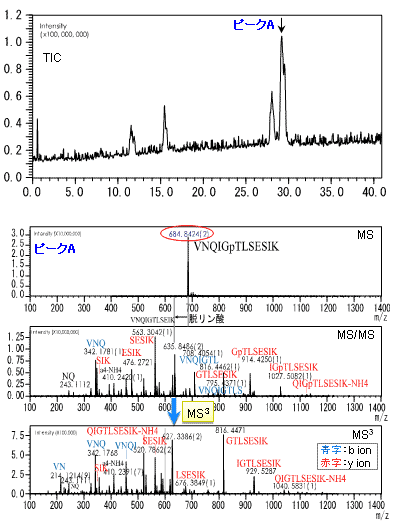
リン酸化部位解析
ピークAをVNQIG
pTLSESIKと帰属
脱リン酸したイオン(2価のため-49)のMS3分析で得られたプロダクトイオンをペプチドの配列に帰属した。
MS/MS分析ではリン酸が脱離していないプロダクトイオンが観測されているため両者のマススペクトルを比較することによりリン酸化部位を6番目のスレオニンと決定した。
NLSを用いたMS3分析は、タンパク質のリン酸化部位の推定に有効であることが示された。
カテゴリー
ライフサイエンス , バイオ
分類
糖